论文题目:Thermoresponsive Polypeptide Fused L-Asparaginase with Mitigated Immunogenicity and Enhanced Efficacy in Treating Hematologic Malignancies. (热响应的多肽融合L-门冬酰胺酶能够降低免疫原性并增强对血液恶性肿瘤的疗效)
文章类型:Research article
影响因子:17.5
文章简介
2023年6月4日,北京大学跨学部生物医学工程系高卫平教授团队筛选出一种类弹性蛋白多肽修饰的抗癌药物门冬酰胺酶(ASP),极大改善了原药的体内药学特性,增强了抗癌效果。
治疗血液学恶性肿瘤的有效药物ASP具有高免疫原性、高毒性、短半衰期和低稳定性,常需要加以修饰。本研究采用类弹性蛋白多肽(ELP)对ASP进行修饰,创新性地采用AlphaFold2对多种ASP-ELP融合产物进行结构预测以预估ELP链对ASP的覆盖程度,由此筛选出两种能够降低免疫原性和保留生物活性的ASP-ELPs候选分子(ASP-ELP60和ASP-ELP90)。实验发现,ELP独特的温敏性使药物在注射后原位形成具有零阶释放动力学的持续释放库,能够显著延长药物半衰期;与ASP和已上市的修饰后药物Oncaspar相比,ASP-ELP90的活性和稳定性高、半衰期长、免疫原性和毒性低,在白血病或淋巴瘤小鼠模型中的疗效显著提高。
该研究发表于国际高水平期刊《Advanced Science》。
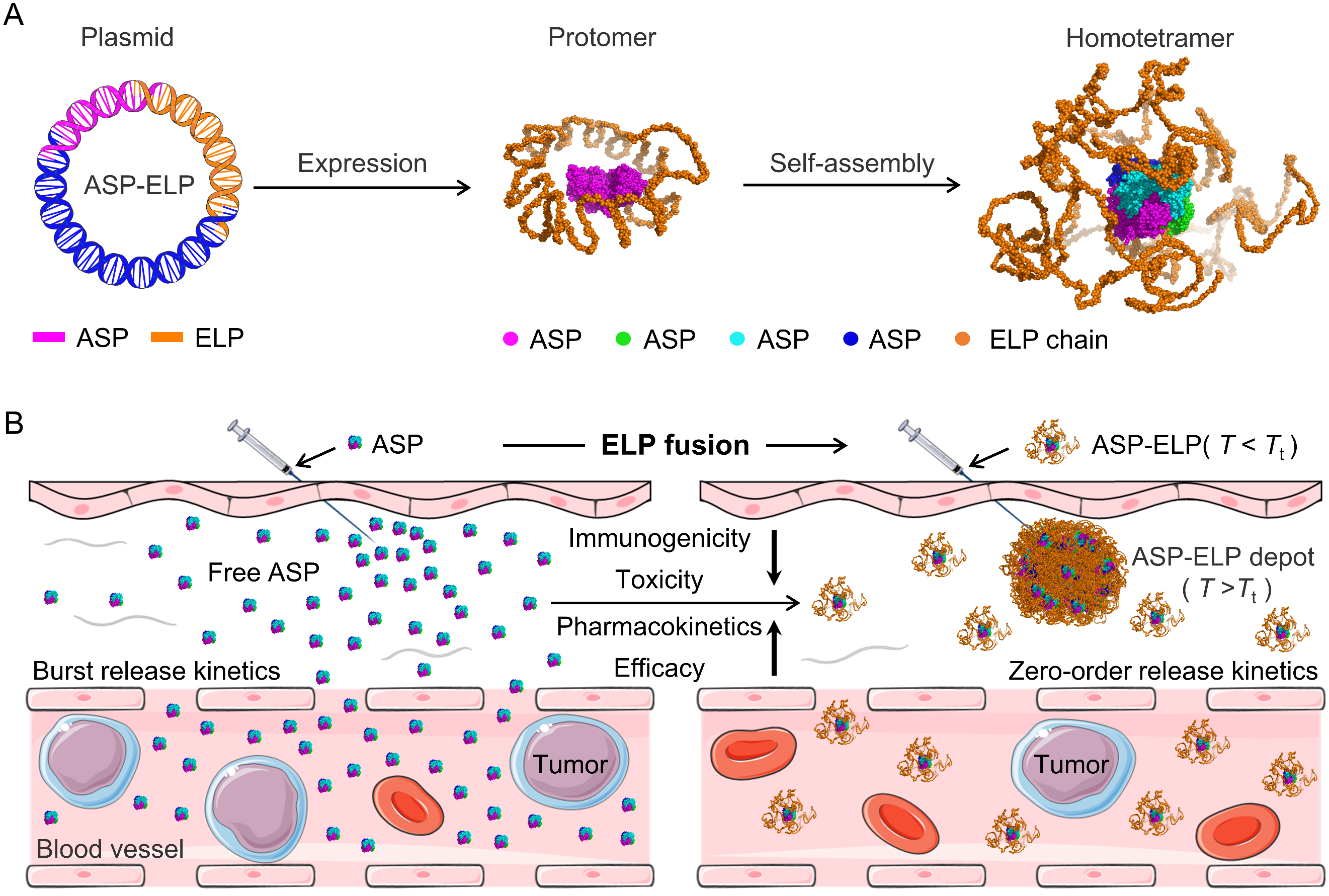
图1. ASP-ELP的合成及体内作用机制。A) ASP-ELP的生物合成和结构预测。ELP链包裹在ASP四聚体表面形成壳核结构,掩盖了ASP的抗原表位,使ASP-ELP具有低免疫原性和高稳定性。B) ASP-ELP的体内药学特性。ELP独特的热敏性使它在注射后原位形成持续释放的药物储库,增强了药代动力学,减轻了与高血药浓度相关的毒性。作者简介

高卫平,北京大学-云南白药国际医学研究中心、北京大学国际癌症研究院、北京大学医学技术研究院、北京大学跨学部生物医学工程系研究员、博士生导师。北京大学化学与分子工程学院博士,日本京都大学化学研究所、美国杜克大学生物医学工程系博士后。现任北京大学跨学部生物医学工程系生物材料与药物递送课题组组长。在PNAS、JACS、Angew、AM等上发表了近60篇SCI论文。已有5项国内外发明专利转让于美国公司Gateway Biotech, Inc.和中山华梓生物科技有限公司。曾多次获Bayer Investigator Award、Janssen Investigator Award、清华大学优秀博士学位论文指导教师奖。承担或参加多项国自然重大、重点、面上项目。



